鉅大LARGE | 點擊量:831次 | 2018年10月07日
電池的負極表面材料分析
由于不做功但是必不可少的電解質以及其他輔助材料的存在,電池的能量密度被稀釋了。
這些額外重量到底有多少??
電解質的重量一般占電池全重15%(鏈接找不到了)隔膜沒查到。估計把外殼,外接電極之類的輔助材料都算上,總重應該不超過電池總重的50%。
不對啊,電池雖然摻‘水’了,但也不至于水得如此啊。市面上的鋰離子電池們的能量密度也就單質鋰的1%左右。這到底又發生了什么?
假如我們認為這兩個電子的做功是一致的,那么就可以估計一下這兩種能量載體的能量密度之比了。
電池能量密度:燃料能量密度=(0.5/170)/(1/6.9)=2.03%電池完敗。
考慮到電池有一半重量是輔助材料,我剛才沒算進去。于是還得打個折。就剩下1%了。
所以能量密度就成了這樣:鋰43.1MJ/Kg鋰離子電池0.36~0.875MJ/Kg
接下來我們的問題是:為什么電池的化學反應要那么復雜,直接降低了電池的能量密度。
這個問題展開說會比較復雜,估計大部分人沒耐心看完。所以先給個簡單答案:
開始長篇之前再放張圖:
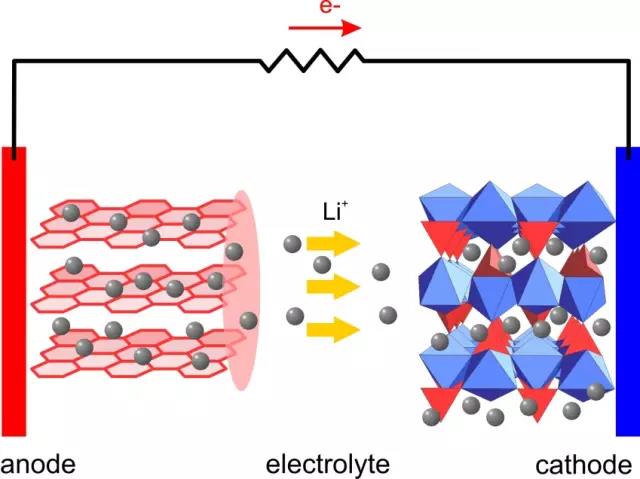
負極的任務很簡單,放電時保證鋰原子(不是離子)都在負極表面失去電子,充電時再把它們抓回來就好了。由于充電時陽極電壓低,帶正電的鋰離子會自發向負極移動,得到電子回歸為鋰原子。
如果是一次性電池,確實不需要石墨。但如果是可充放電池,陽極表面材料不是石墨也會是其它物質。
我們都知道所有金屬都是良好電子導體,鋰是金屬,所以鋰是良好電子導體。于是先到負極的鋰原子成為了負極的一部分,于是后到負極的鋰離子加入了前鋰的行列。。。。
于是完全由鋰原子構成的晶體出現了。這個過程,又稱析晶。結果是鋰晶體會刺穿隔膜到達正極,于是電池短路報廢了。
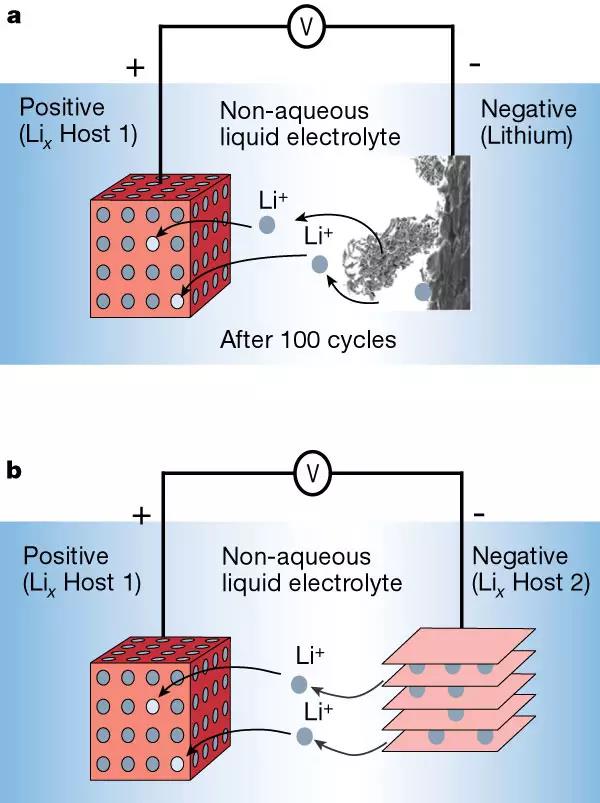
對于析晶這一現象,我們可以這么理解。
在充電過程中,我們對于鋰離子的控制實際上很弱。我們只能保證鋰離子會移動到負極表面,但我們無法保證鋰離子會均勻地分布在負極表面。因此在沒有外來約束條件下,充電時鋰晶體會在負極表面無序生長,形成枝晶(dendriticcrystal)。
所以一定要有個約束條件。要挖個坑讓鋰離子往里面跳。
這個坑的具體表現即為負極表面的石墨材料。如上圖所示,石墨層之間的空隙夠大,足以容納單個鋰原子,但也只能容納單個鋰原子;然后石墨層與鋰原子之間的物理吸附作用可以穩住鋰原子,于是鋰原子在沒有外來電壓時候也能安心待在負極表面。
下一篇:關于電池的正極表面材料分析

























